Observe o diagrama de energia e os exemplos de distribuição eletrônica já estudados em aulas anteriores e resolva os exercícios seguintes.
Diagrama de Energia ou Diagrama de Linus Pauling
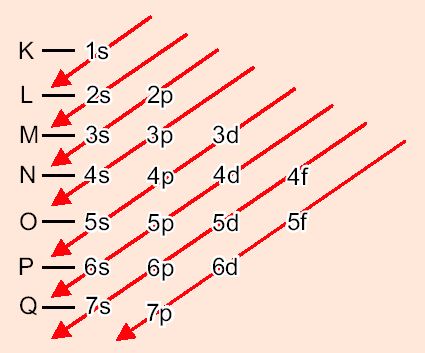

1-Qual a soma dos números de elétrons dos subníveis 2p dos seguintes átomos: 3Li, 5B, 6C, 7N, 16S?
R:
2-O subnível 4s1 é o mais energético de um átomo. Determine:
a) o número total de elétrons desse átomo;
R:
b) o número de camadas.
R:
3-Escreva a quantidade de elétrons em cada camada eletrônica:
camada K:
camada L:
camada M:
camada N:
camada O:
camada P:
camada Q:
4-Qual o número atômico do elemento que possui na última camada eletrônica os seguintes subníveis 4s2 4p5?
R:
4-Escreva a distribuição eletrônica por subnível do elemento Carbono, que tem número atômico 6:
5-Para saber a quantidade de camadas eletrônicas que um determinado elemento tem, basta ver a linha horizontal da classificação periódica que ele está localizado. Considerando isso, responda:
a)Um determinado elemento está na sexta linha horizontal da tabela periódica. Quantas camadas esse elemento apresenta?
b)Um determinado elemento está na quinta linha horizontal da tabela periódica. Quantas camadas esse elemento apresenta?
c)Um determinado elemento está na quarta linha horizontal da tabela periódica. Quantas camadas esse elemento apresenta?
d)Um determinado elemento está na terceira linha horizontal da tabela periódica. Quantas camadas esse elemento apresenta?
e)Um determinado elemento está na segunda linha horizontal da tabela periódica. Quantas camadas esse elemento apresenta?
6-Quantas camadas eletrônicas existem no?
a) Ca
b) Na
c) Mg
d) Xe
e) Fe
f) Zr
g) P
h) Rn
i) N
j) In
7-Escreva a distribuição eletrônica por subnível do elemento enxofre, que tem número atômico 16:
8-Analise o elemento que apresenta número de massa 31 e 16 nêutrons e responda os quesitos a seguir:
a)Qual o seu número atômico?
b)Qual a sua distribuição eletrônica por subnível?
c)Quantas camadas esse elemento tem?
d)Qual é a sua última camada (em letra: K, L, M, N, O, P, Q)?
9-Considerando que o subnível mais energético é o último subnível distribuido, qual o subnível mais energético do elemento ferro, que apresenta número atômico 26?
10-Qual o número atômico de um átomo, sabendo que o subnível mais energético (último subnível distribuído) da sua distribuição eletrônica no estado fundamental é o 4p2?
11-Qual a configuração eletrônica por subnível em ordem de energia do elemento escândio (Sc), que apresenta número atômico 21?
12-Escreva o número de elétrons que o elemento Bromo (Br) apresenta na última camada eletrônica (denominada camada de valência):
13-Um átomo tem número de massa 31 e 16 nêutrons. Qual é o seu subnível mais energético (último subnível distribuído)?
14-Determine o número atômico de um elemento que apresenta três níveis de energia e seis elétrons no último nível (denominado nível de valência):
15-Quantas camadas eletrônicas existem no elemento químico de número atômico tungstênio, de número atômico 74?
16-Quantos elétrons podem ter no máximo no
a)subnível s?
b)subnível p?
c)subnível d?
d)subnível f?
17-Qual o número atômico de um determinado elemento que apresentou a seguinte distribuição eletrônica por subnível?
a)1s2 2s2 2p6 3s2 3p64s2 3d7 - número atômico:
b)1s2 2s2 2p6 3s2 3p6 4s2 3d4 - número atômico:
18-Escreva a distribuição eletrônica por subnível do elemento de número atômico 31:
19-Escreva a distribuição eletrônica por subnível do elemento de número atômico 55:
e responda:
a)Qual o número de elétrons em subnível s?
b)Qual o número de elétrons em subnível p?
c)Qual o número de elétrons em subnível d?
d)Quantas camadas esse elemento apresenta?
e)Qual a letra que representa a última camada?